Терапия атеросклероза
Атеросклероз. Общая информация
Патогенез
Патогенез атеросклероза называют атерогенезом. Развитие атеросклеротического поражения — это совокупность процессов поступления в интиму и выхода из неё липопротеидов и лейкоцитов, пролиферации и гибели клеток, образования и перестройки межклеточного вещества, а также разрастания сосудов и обызвествления.
Рисковые факторы, такие как курение, повышенное содержание холестерина в плазме, артериальное давление способствуют тому, что в интиме сосудов накапливаются липопротеины низкой (ЛНП) и очень низкой плотности (ЛОНП), которые проникая в эндотелиальные ткани сосуда привлекают макрофагов. Если накапливается очень много липидов внутри эндотелиальной ткани, то макрофаги поедая большое количество липопротеинов превращаются в так называемые пенистые клетки. Эта начальная стадия приводит к тому, что образуется атеросклеротическая бляшка. Внутри атеросклеротической бляшки создаются условия для клеток эндотелия при которых они откладывают кальций на поверхности бляшки. В результате этих процессов стенки сосуда увеличиваются и становятся более жесткими. Образования на сосудах сужают просвет приводя к повышению артериального давления и образованию новых микротравм. Повышение артериального давления способствует новым повреждениям сосудов, при повышенном содержании ЛНП в плазме они снова становятся источником новых липидных бляшек, что в дальнейшем приводит к разрушениям системно-важных артерий, служит причиной инсультов и инфарктов.
Роль холестерина
Традиционно считают, что повышенное содержание холестерина в крови является рисковым фактором для развития атеросклероза, однако новые данные о метаболизме липидов или триглицеридов (ТГ) говорят о том, что следует различать хороший холестерин, содержащийся в липопротеинах высокой плотности (ЛВП), и плохой холестерин, который несут другие липопротеины, преимущественно липопротеины низкой плотности (ЛНП). Кроме того, было выявлено, что атеросклероз может развиваться и у людей с нормальным уровнем общего холестерина в крови, поэтому этот показатель не так однозначен.
Роль холестерина при атерогенезе раньше сводилась к тому, что он является составным компонентом транспортной системы липидов, способствуя более высокой концентрации ТАГ в плазме и его нахождение в кровеносной системе ассоциировалось с более высоким риском образования атеросклеротических бляшек. Сейчас стало понятно, что холестерин входящий в состав ЛВП приводит к повышению выведению липидов из плазмы, и является позитивным фармакодинамическим параметром, а в составе ЛНП он приводит к обратному эффекту, повышая концентрацию ТАГ в крови. Поэтому для выбора оптимальной терапии атеросклероза необходимо понимать в чем состоит роль холестерина в метаболизме ТАГ:
1). В ходе транспорта липидов
2). В процессах обратного транспорта липидов
Кроме того, холестерин необходим для выработки витамина D, выработки надпочечниками различных стероидных гормонов (включая кортизол, альдостерон, половые гормоны: эстрогены, прогестерон, тестостерон), жёлчных кислот. Он является важным компонентом мембран всех животных и растений, придавая ей необходимую устойчивость. Поэтому сам по себе холестерин не вреден, а очень важен и нужен. Однако на его функциях мы будем остановимся только применительно к липидам.
Транспорт липидов
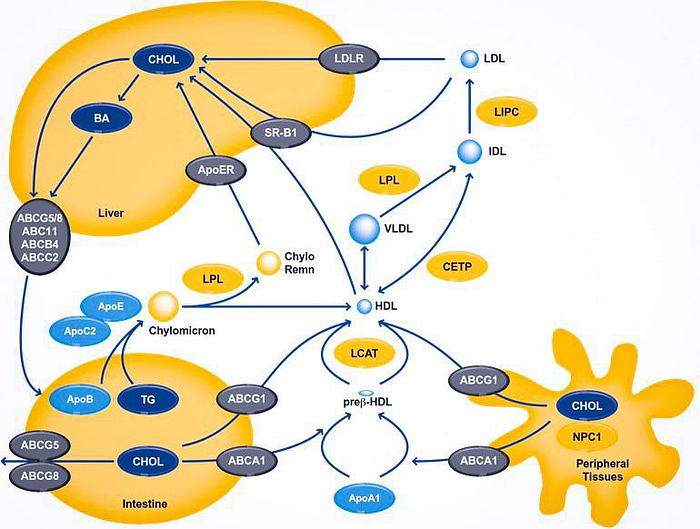
Для понимания работы транспортной системы, выбора оптимальных молекулярно-генетических маркеров, а также выбора собственно терапевтических средств, следует разобраться с основными компонентами транспортной системы липидов.
Первое, основным депо холестерина является печень, которая является местом метаболизма и синтеза холестерина. Второе, основные участники, которые играют роль в этом метаболизме среди липопротеинов — это ЛВП (HDL) (через него пролегают все пути обратного транспорта триглицеридов (TG) в печень) и ЛНП (LDL) — они являются другим узким местом системы метаболизма и по ним оценивают прямой транспорт из печени в другие органы и ткани.
Для последующего выбора терапии для нас важно, понимать выведение и образование этих двух компонентов транспортной системы и понимать прямую и обратные связи между этими процессами.
HDL представляет собой липопротеин с крайне низким содержанием липидов в своем составе с преобладанием холестерина, его там на порядок больше, чем триглицеридов. Он преобразуется в LDL путем всасывания жиров с помощью LPL и CETP, а также пассивно может преобразовываться в IDL за счет всасывания жиров напрямую из кавеол, однако значимость этого довольно мала по сравнению со всасыванием опосредованно через рецепторы, поэтому мы можем сказать, что LDL находится в системе прямой-обратной взаимосвязи с LDL.
Также, важно отметить, что имеется два пути вывода LDL из плазмы обратно в печень — через LDLR и через SR-B1, однако клиническое значение имеет первый путь, потому что он приводит к понижению концентрации LDL и не оказывает прямого воздействия на концентрацию HDL.
Клинические исследования
Подбор модальности терапии
В ходе 3-ех десятков лет, понижение уровня LDL-Холестерина показало убедительный эффект на течение атеросклероза. Статины, как наиболее известные представители класса LDL-C понижающих средств достаточно эффективны, однако проблемы с побочными
эффектами, с недостаточной эффективностью в некоторых группах пациентов заставляют разрабатывать новое лекарство и увеличивать эффективность понижение LDL-C.
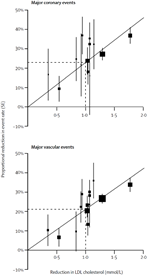
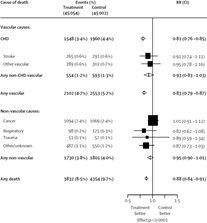
Для начала, хотелось бы подтвердить данное утверждение небольшими статистическими показателями, полученными в ходе исследования на 90 056 пациентах. Они представлены на рисунках 1, 2, 3 выше. Во-первых, понижение уровня LDL-C оказывало влияние не только на понижение уровня смертности до 83% от контроля, но и на понижение уровня общей смертности до 88% от контроля. Кроме того, линейная аппроксимация эффекта от концентрации LDL-C в плазме показала, что при понижении LDLC до нулевого уровня сводит к нулю риск возникновения нежелательных сердечно-сосудистых событий.
Статины
Статины, как уже было упомянуто ранее приводят к различным побочным. Наиболее важные из долгосрочных эффектов это повышение риска возникновения сахарного диабета, краткосрочные же эффекты сильно варьируют в зависимости от выбранного типа статинов, но хорошо доказано, что статины являются причиной повышения риска возникновения миалгии на 7%, а также приводят к значительному повышению креатинового клиренса на 13% и более (до 1624% по сравнению с контролем), что является огромной нагрузкой на печень.
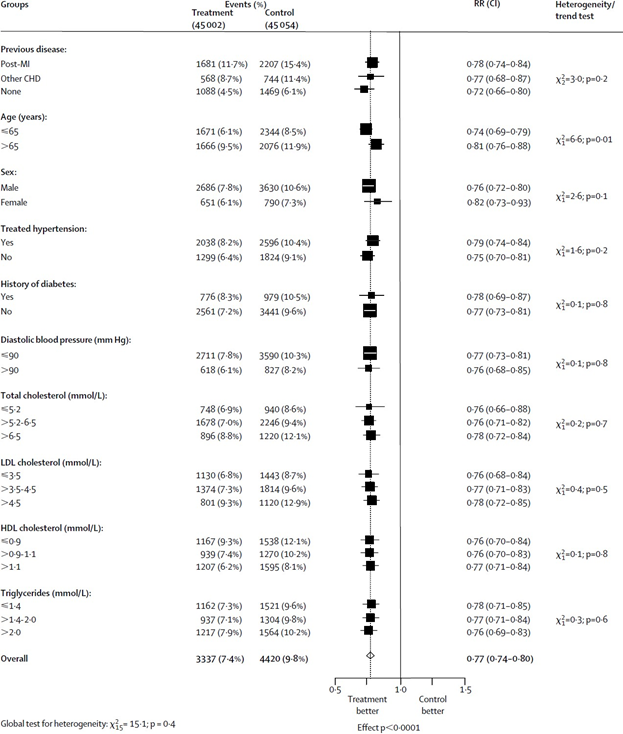
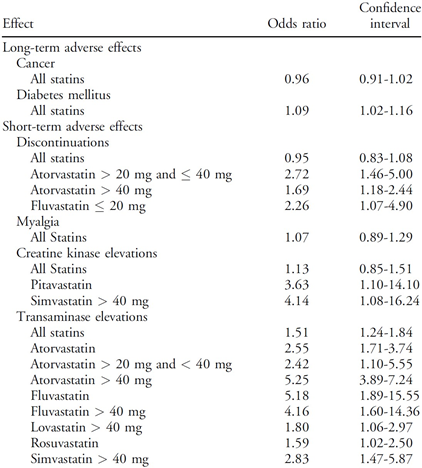
Все это приводит к миопатии и так называемой гиперККемии — патологии хронического нарушения креатинового клиренса, которая вынуждает отменять прием статинов, для пациентов с обнаруженными симптомами. Механизмы, которые приводят к побочным эффектам до сих пор не до конца изучены, предварительно полагают, что статины воздействуют на нормальную митохондриальную функцию, ниже приведены возможные цели, по которым статины нарушают работу митохондрий.

Все это показывает, что на данный момент не до конца понятна роль статинов и поэтому требуются альтернативные варианты терапий, одна из которых — это ингибирование PCSK9.
Ингибиторы PCSK-9
С открытия в 2003 пропротеин конвертазы субтилизин/кексиного типа 9 (PCSK9) привело к изменению в направлении клинических исследований по лечению атеросклероза.

Критически важное исследование, проведенное в 2006 обнаружило, что ответственный за взаимодействие LDL-C с LDLR и приводящий к деградации LDL-рецепторов PCSK9 при ингибировании его антителами приводит к резкому понижению уровня LDL-C. Альтернативные методы внутрипеченочного ингибирования PCSK9, такие как сайленсинг PCSK9-транскрипции и малые молекулы-ингибиторы, разрабатываются в данный момент.
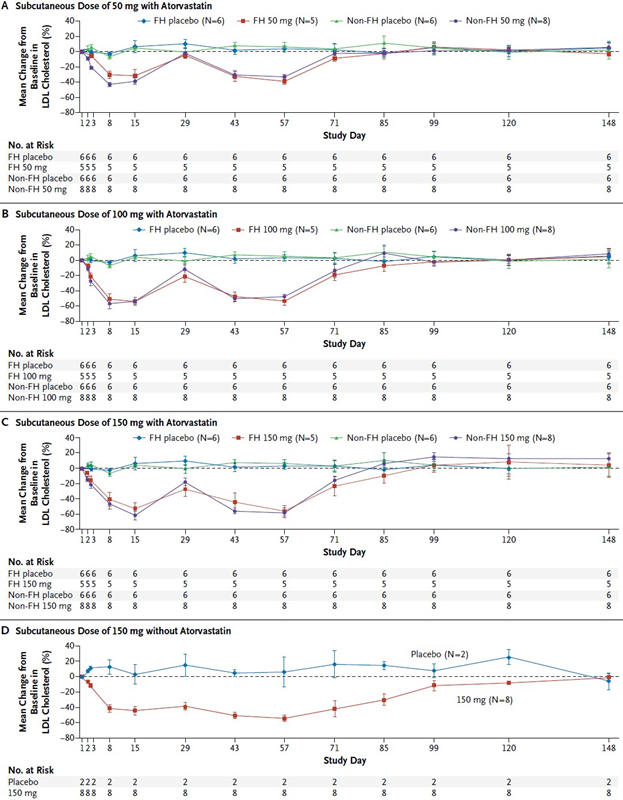
Фармакокинетические и фармакодинамические данные при лечении с помощью эволокумаба (AMG 145 Ab) приведены ниже на рисунке 4 показывают насколько эффективна данная терапия.
В ходе клинических исследований также выявлено, что терапия при помощи статинов не является причиной несовместимости приема ингибиторов PCSK9, напротив — прием антител к PCSK9 приводит даже к небольшому синергетическому (или аддитивному) эффекту, что показано на рисунке ниже, где сравниваются результаты приема ингибитора PCSK9 вместе с терапией с помощью аторвастатином и без таковой. Видно, что при приеме вместе с аторвастатином концентрация LDL-C понижается на 65% относительно плацебо, однако без аторвастатина наблюдается более стабильный эффект понижения концентрации LDL-C на 60%.
Циклодекстрины
Следующее терапевтическое средство, которое будет очень хорошо комбинировать с понижением уровня LDL-C в плазме это цв плазме это циклодекстрины. Циклодекстрины — углеводы, циклические олигомеры глюкозы, получаемые ферментативным путём из крахмала. Ниже приведены химические формулы трех основных представителей. В связи с тем, что в атерогенезе участвуют также и воспалительные реакции, индуцированные кристаллами холестерина, необходимо также увеличивать растворимость холестерина в плазме, таким образом разрушая кристаллы холестерина и восстанавливая нормальную функцию сосудов.

В работе, опубликованной в этом году устанавливается роль потенциального компаунда для терапии атеросклероза — β-циклодекстрина.

На рисунке видно, что нормальная картина для работы сердечно-сосудистой системы восстанавливается при приеме циклодекстринов: разрушаются кристаллы холестерина, уменьшаются размеры бляшки, при этом количество кристаллов в бляшке сокращается, что приводит к уменьшению воспалительной реакции через макрофаги и понижению продукции ROS в аорте.